文章转载:非科学美妆传播公众号
 贝泰妮这篇美白成分验证的文章,说实话看得我有点迷。
贝泰妮这篇美白成分验证的文章,说实话看得我有点迷。
文章一方面认为,CA是熊果苷的衍生物,其美白功效是承袭自熊果苷:
①文章开头是通过熊果苷(AR)引入6′-O-咖啡酰熊果苷(CA) ,那意思是CA作为常用美白剂熊果苷的衍生物,我推测CA也可以美白,且多了酯键连接咖啡酸的保护,能减少一些AR存在的安全性问题(容易糖苷水解变成氢醌)。
②讨论部分第一段说的更直白: 直接讲CA是作为AR和咖啡酸的“前药Prodrug”。那作为前药,那就是认为你得在进入体内后分解了才能发挥作用。

但文章另一方面,又证明了CA的美白通路与熊果苷传统的抑制酪氨酸酶完全不同。那如果还坚持“前药”的观点,文章主角CA的这条「干扰MITF二聚化」的美白“新”通路,熊果苷、咖啡酸能不能起到类似的作用呢?文章中没有做相关验证。
再多深入问下去,文章通过CA不会被酶解的实验强调CA很稳定,但两种水解方式的验证都只是单独进行的。如果是级联反应呢?
最后看了一下CA这颗原料,除了贝泰妮给它做美白验证,最近还有很多其他护肤之外的功能验证。找了贝泰妮的专利,好像也没看到写这颗原料的。结合文章的funding单位,感觉是不是贝泰妮接了一部分这个funding的指标呀😅😅
——————
以下是这篇关于6′-O-咖啡酰熊果苷(CA)的美白功效研究文献的详细解读:
—-
一、研究背景(Introduction)
①行业痛点:
• 熊果苷(Arbutin, AR)是化妆品中最常用的美白活性成分之一
• 安全性危机:AR在体内可降解为氢醌(Hydroquinone, HQ),后者具有皮肤刺激性、致敏性,甚至可导致白斑病(leukoderma)和外源性褐黄病(ochronosis)
• 监管收紧:欧盟委员会法规2024/996已将α-和β-熊果苷列入化妆品限制使用清单,要求HQ含量不得超过不可避免的痕量水平
②技术瓶颈:
• AR衍生物化是提升稳定性的有效策略,但多步复杂的化学合成限制了其工业化生产
• 亟需开发天然来源、结构稳定、低毒性的AR替代物
研究契机:
• 6′-O-咖啡酰熊果苷(6′-O-Caffeoylarbutin, CA) 是一种天然多酚化合物,主要存在于越橘属植物Vaccinium dunalianum Wight的花蕾中
• CA由咖啡酸与AR通过酯键连接而成,理论上可通过共轭效应和空间位阻保护糖苷键,抵抗水解生成HQ
—-
二、研究目的(Objectives)
1. 验证CA的结构稳定性:通过化学水解和酶解实验,比较CA与AR的降解行为及HQ生成量
2. 评估长效美白功效:利用斑马鱼撤药模型验证CA的持续抑黑效果
3. 阐明分子机制:探究CA调控黑色素生成的具体靶点和信号通路
—-
三、研究方法(Methods)
①材料制备:从V. dunalianum花蕾中经乙醇提取、D101大孔树脂分离、硅胶柱层析、Sephadex LH-20纯化获得CA(纯度98%)
②结构鉴定:¹H NMR和¹³C NMR核磁共振波谱
③稳定性测试:HPLC-DAD检测,定量分析HQ生成量:1)1M HCl酸性水解;2)β-葡萄糖苷酶酶解(37°C, 24h)
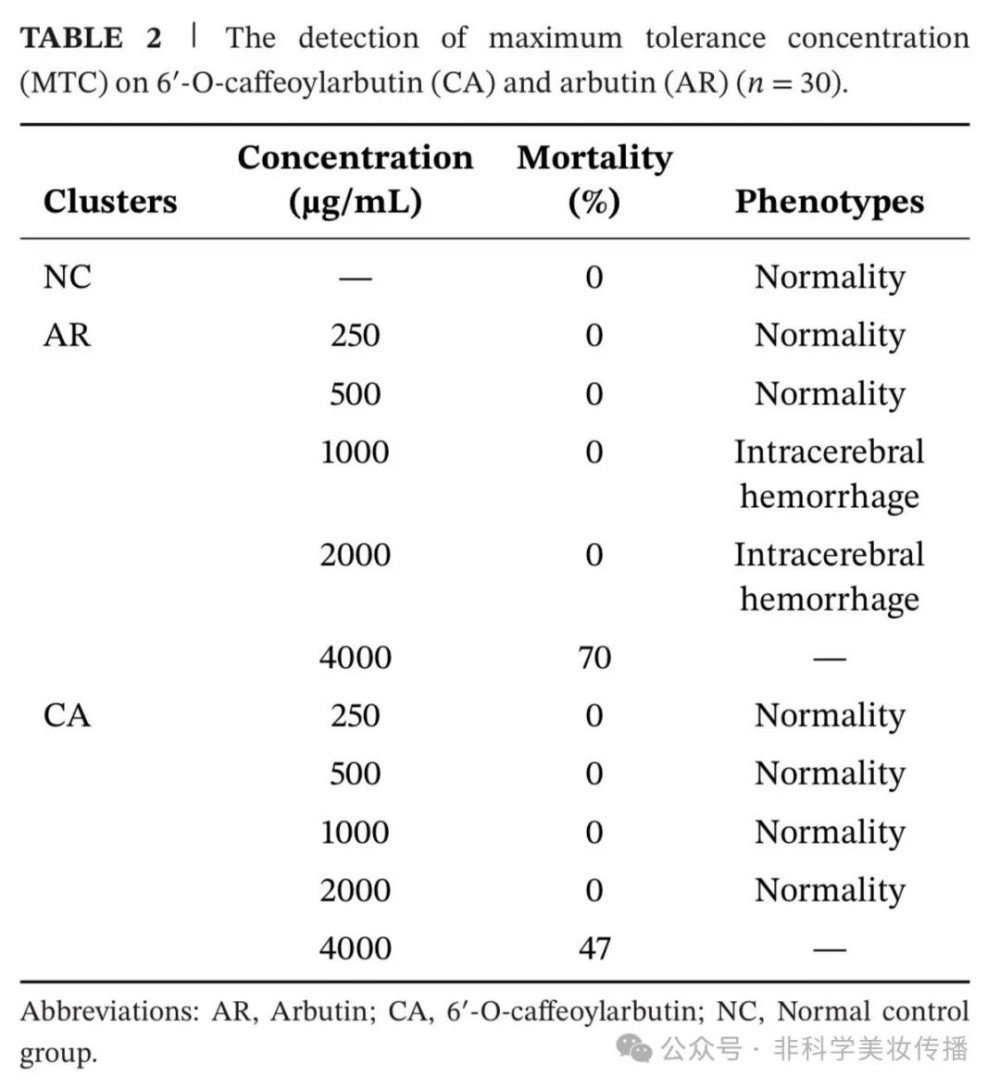
④动物实验:斑马鱼(AB品系)最大耐受浓度(MTC)测定;撤药模型(48h给药后撤药,追踪0-108h黑色素恢复情况)
⑤细胞实验:SK-MEL-1人黑色素瘤细胞:CCK-8毒性检测;RT-qPCR检测14个黑色素生成相关基因;Western blot检测MITF、PMEL蛋白
⑥超微结构:透射电镜(TEM)观察黑色素体(melanosome)形态和数量
⑦分子对接:AutoDock Vina将CA与MITF的bHLH-LZ结构域(PDB: 7D8T)对接,与已知抑制剂TT-012对比
—-
四、研究结果(Results)
4.1 稳定性优势——CA显著优于AR
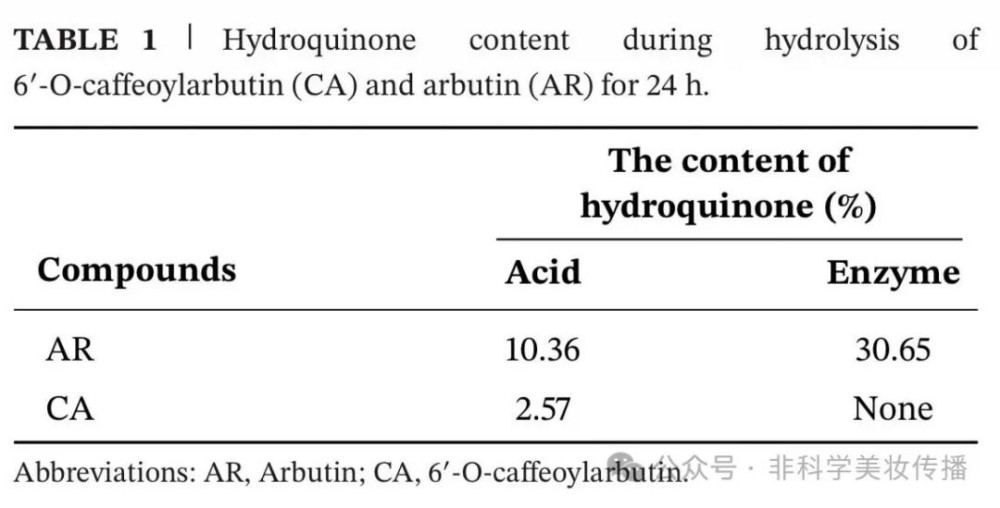
①酸性水解(1M HCl)
• AR完全水解为HQ;CA先水解释放咖啡酸+AR,再缓慢释放HQ
• CA: 2.57% vs AR: 10.36%
②酶解(β-葡萄糖苷酶)
• AR30.65%转化为HQ;CA几乎不降解
• CA: 未检出 vs AR: 30.65%
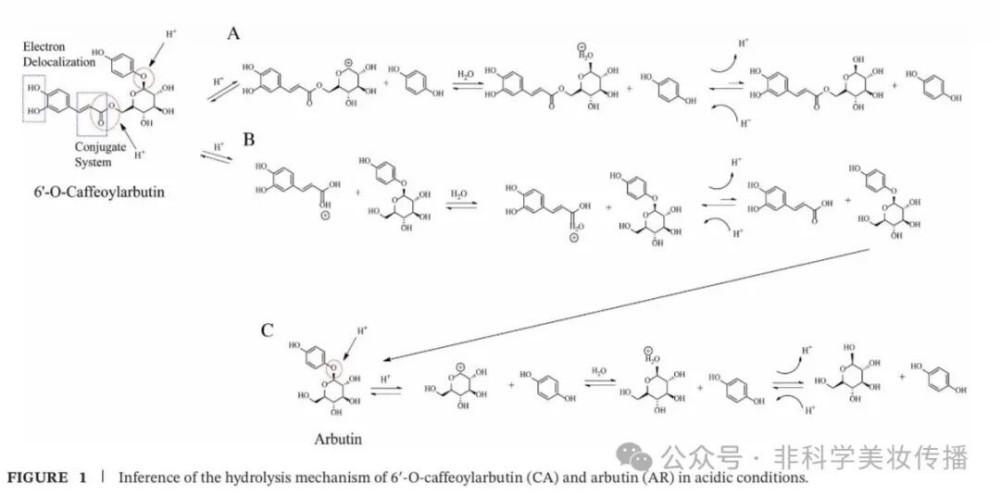
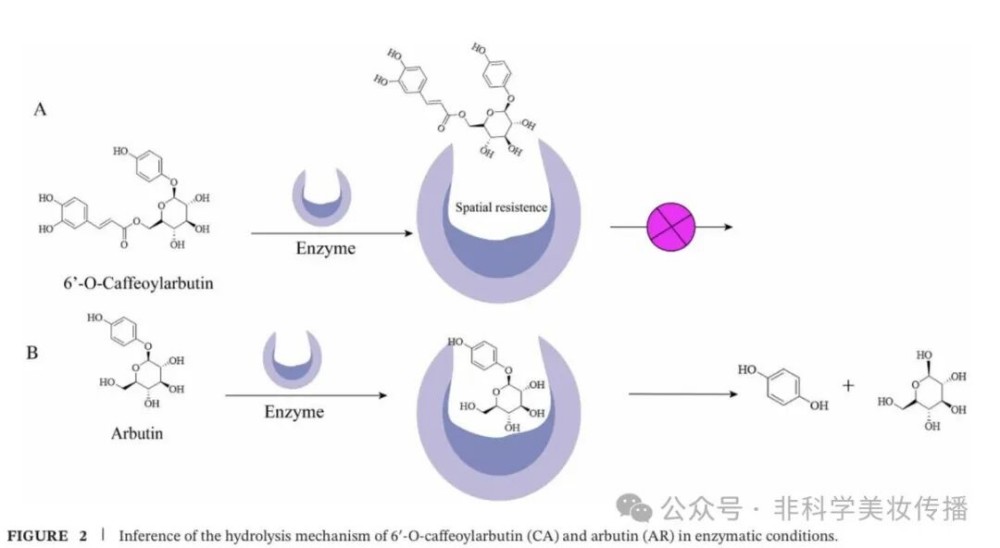
③机制解释(图1-2):
• 共轭保护:咖啡酰基的羰基与烯烃形成共轭体系,阻止H⁺攻击糖苷键
• 空间位阻:大分子咖啡酰基阻碍酶进入催化位点
4.2 长效抑黑功效——斑马鱼撤药模型
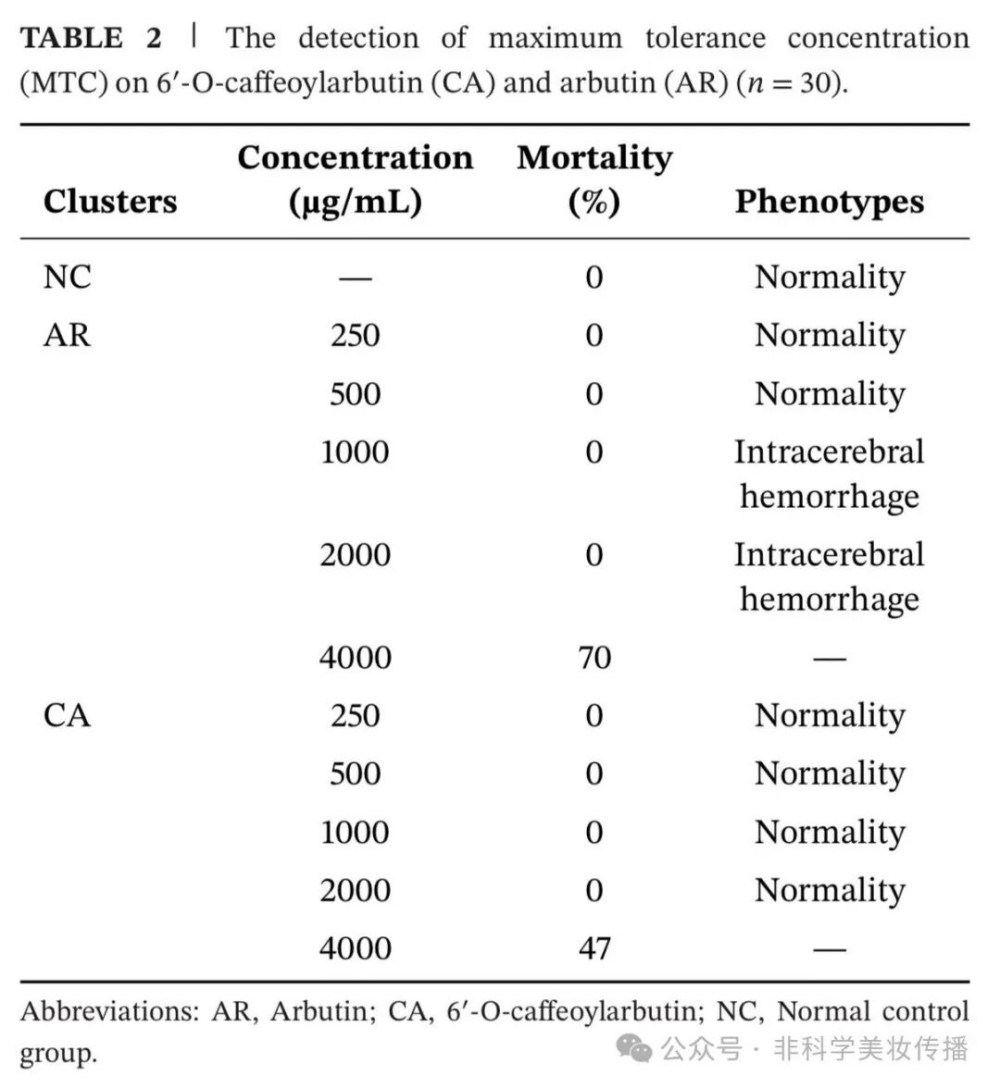
安全性:CA的MTC(2000 μg/mL)是AR(500 μg/mL)的4倍,毒性更低
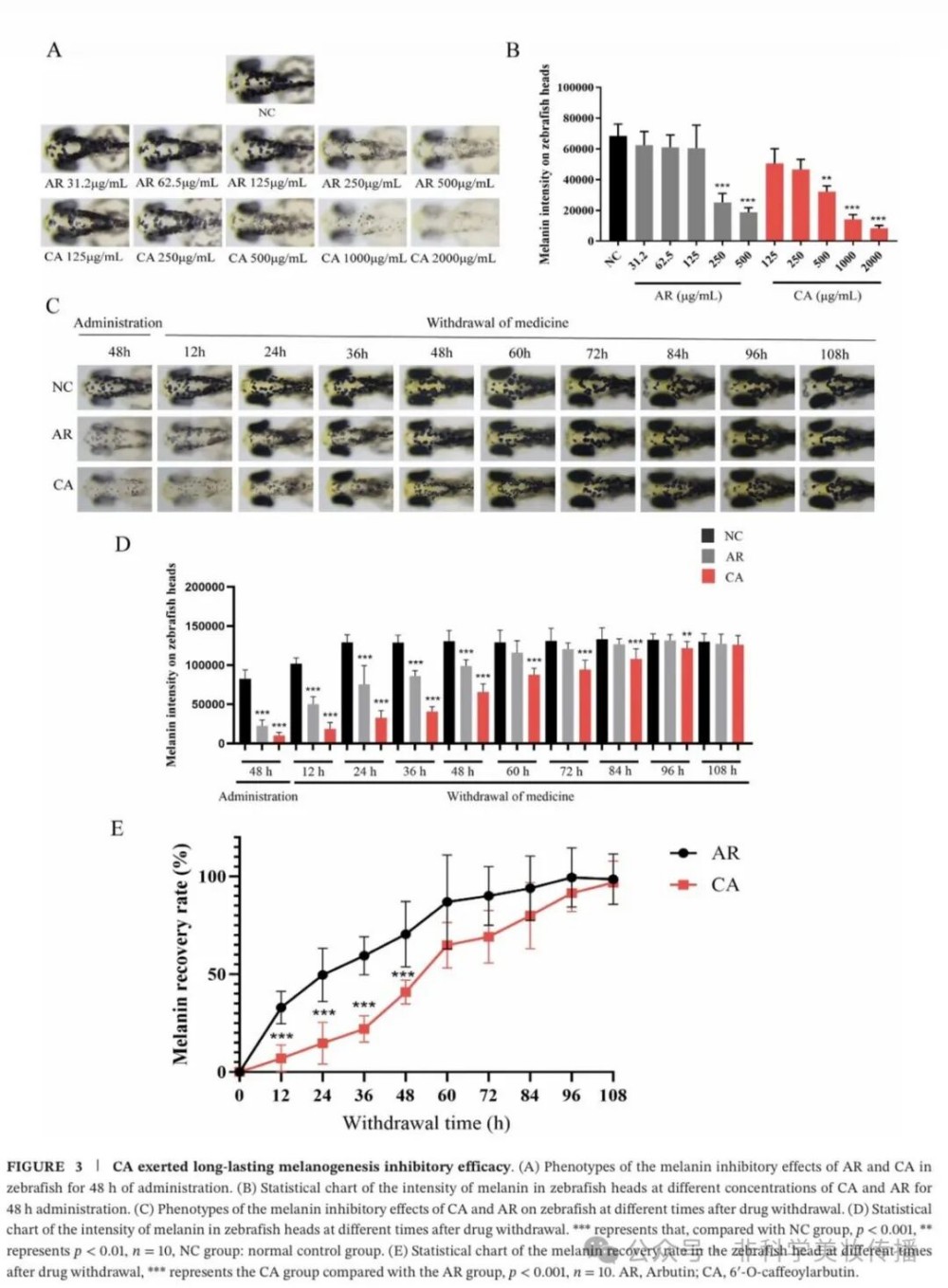
抑黑持续性(图3):
• 撤药后黑色素恢复率:CA组显著低于AR组(12h-48h, p<0.001)
• 药效减半时间:AR为撤药后24h,CA延长至48h
• 表明CA具有长效抑黑特性
4.3 分子机制——靶向MITF调控黑色素体成熟
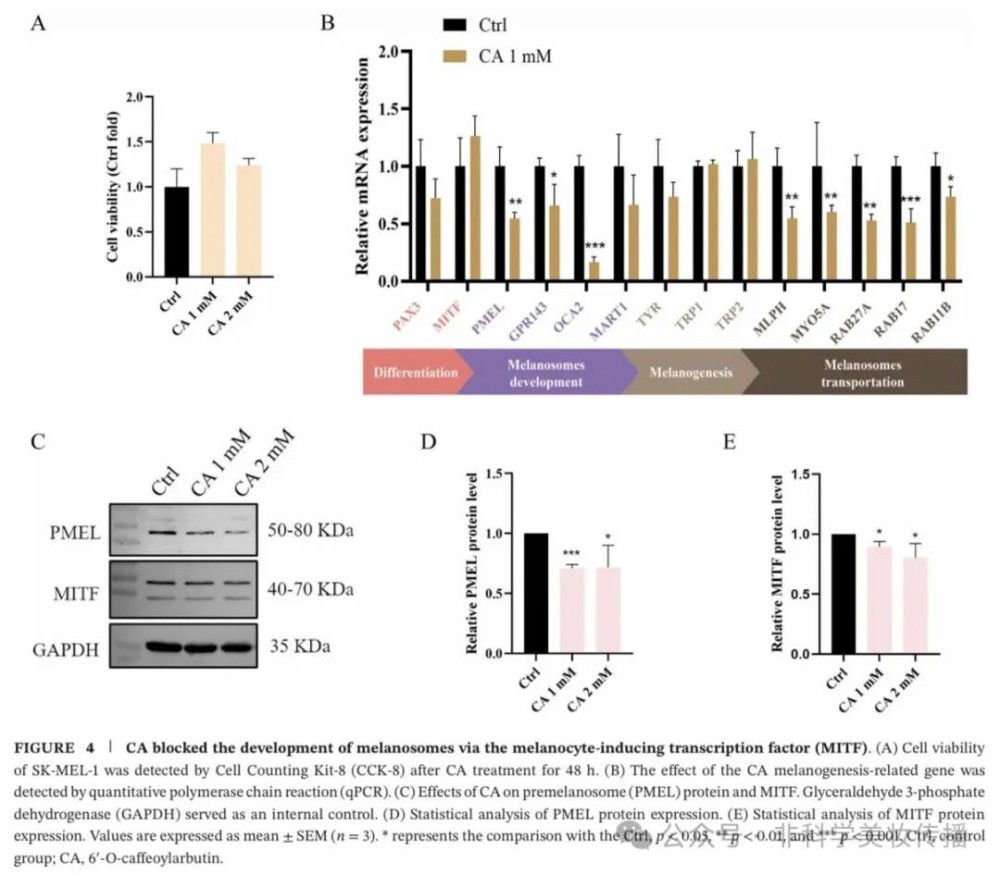
①基因表达谱(图4):
• 显著下调(p<0.05):黑色素体发育基因(PMEL, OCA2, GPR143)和转运基因(RAB27A, RAB17, MYO5A, MLPH)
• 无显著变化:黑素细胞分化核心转录因子(PAX3, MITF)和黑色素合成酶(TYR, TRP1, TRP2)
②蛋白水平:
• PMEL蛋白↓(~50%),MITF蛋白↓(10-20%)
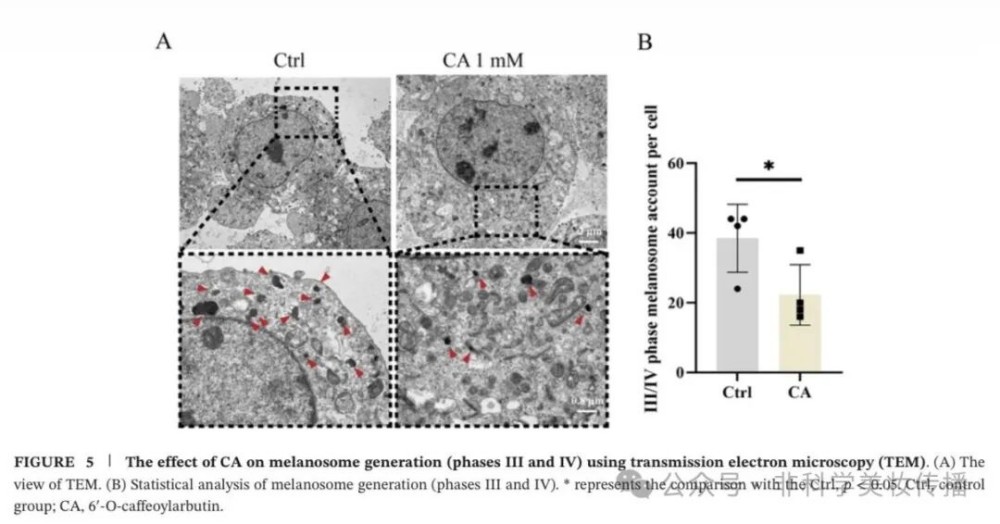
③超微结构(图5):
• TEM显示CA组III/IV期黑色素体(含黑色素的成熟阶段)数量显著减少(p<0.05)
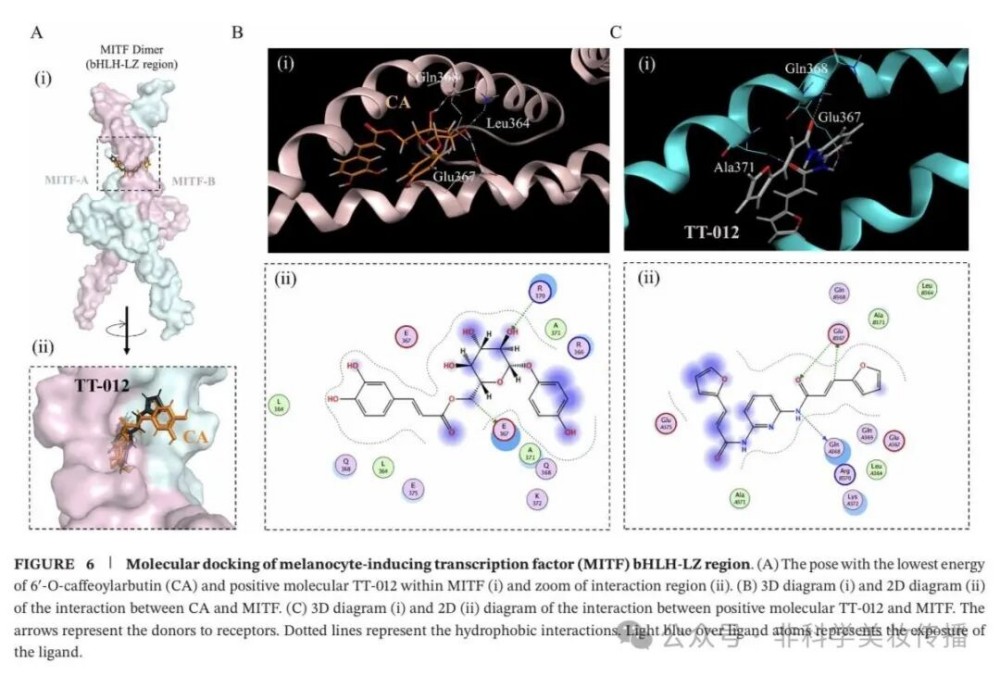
分子对接(图6):
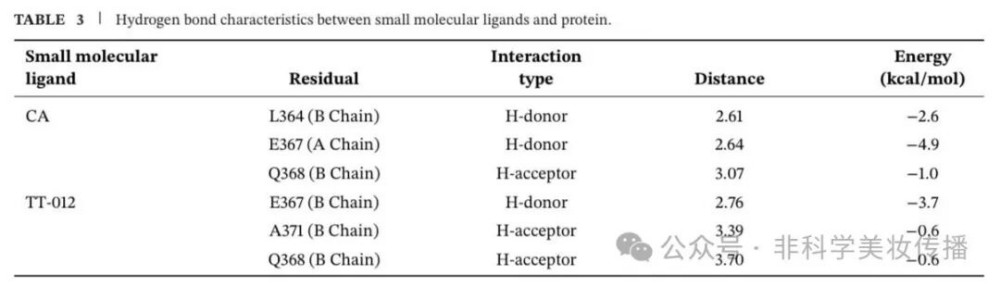
• CA与MITF的bHLH-LZ二聚化结构域结合,结合位点与已知抑制剂TT-012高度重叠
• 形成氢键:Glu-367, Gln-368, Leu-364——这些残基是MITF二聚化和DNA结合的关键位点
• 推测机制:CA干扰MITF二聚化,抑制其转录活性,从而阻断黑色素体成熟
—-
五、讨论(Discussion)
5.1 核心创新点:
① “前药”设计理念:CA作为AR的天然衍生物,在保持美白活性的同时,通过结构修饰实现:
• 酯键保护减少HQ释放(安全性↑)
• 酶解稳定性延长作用时间(长效性↑)
② 独特的作用机制:与传统酪氨酸酶抑制剂(如AR直接抑制TYR)不同,CA通过调控MITF-黑色素体成熟通路发挥作用:
• 不直接抑制黑色素合成酶
• 而是阻断黑色素体的发育、成熟和转运
• 这为美白成分开发提供了新靶点
③ 天然来源优势:从云南特色植物V. dunalianum中直接提取,避免了复杂化学合成,利于工业化
5.2 研究局限性:
• 使用MTC剂量可能高估长效性(实际化妆品使用浓度更低)
• 斑马鱼模型需向哺乳动物/临床转化验证
—-
六、结论(Conclusion)
6′-O-咖啡酰熊果苷(CA)是一种结构稳定、低毒性、长效持久的新型天然美白成分。其通过咖啡酰基提供的共轭效应和空间位阻,显著抵抗水解生成氢醌;在斑马鱼模型中展现出优于AR的持续抑黑效果(药效维持时间延长1倍)。机制上,CA通过干扰MITF二聚化,抑制黑色素体成熟和转运,而非直接抑制酪氨酸酶。CA为开发安全、长效的抗色素沉着化妆品提供了有前景的替代方案。
发稿/咨询/合作联系:13710470565(微信)
相关文章









.jpg)