文章转自:美妆前沿研究|原文链接
皮肤每天都在悄悄更新——表皮最外层的角质细胞不断脱落,新的细胞从基底层补充上来。这个过程我们称之为脱屑(desquamation),它是维持皮肤屏障完整性的基础。我们早就知道,角质层的酸性微环境是启动这一过程的关键,也知道酸性pH会激活角蛋白酶(KLKs)来降解细胞间的桥粒蛋白,从而让角质细胞得以脱落。但有一个核心问题始终悬而未决:角质形成细胞究竟通过什么分子来”感知”酸性信号?
近期发表于PNAS的一项研究给出了答案——质子激活氯离子通道PACC1,正是这个长期被忽视的感受器。

01
在众多候选者中锁定PACC1
皮肤科学界并非不知道角质层存在酸敏感的离子通道,早在2008年就有研究记录了人角质形成细胞在酸性pH下产生氯电流的现象,但这条电流究竟来自哪个通道蛋白,一直没有定论。
研究团队从电生理实验切入。他们在人原代角质形成细胞和HaCaT细胞系中进行膜片钳记录,发现pH 4.6的酸性环境可以诱发强烈的电流反应,而氯离子通道阻断剂尼氟酸(niflumic acid)能显著压制这一反应。关键的排除实验同样清晰:ASIC、TRPV1、TRPV3等已知的酸敏感离子通道的激动剂和拮抗剂均对这条电流没有影响。随后,Western blot确认PACC1在两种细胞中均有丰富表达,而敲低PACC1后酸诱导的电流大幅减弱。至此,PACC1被确立为角质形成细胞中最主要的酸敏感离子通道。
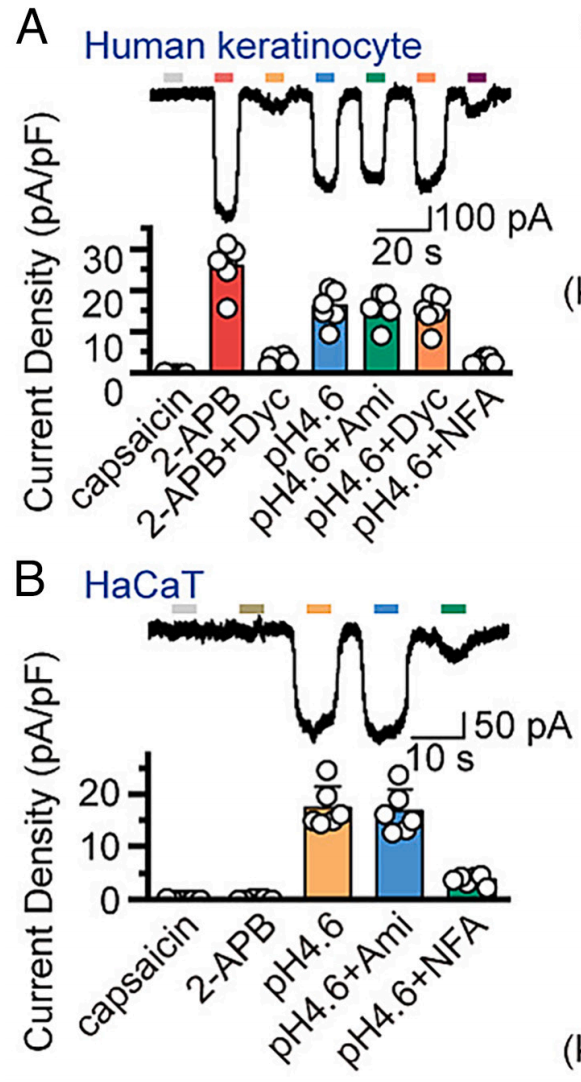
图1.(A)人角质形成细胞中的代表性全细胞记录。Dyc:达克罗宁;Ami:阿米洛利;NFA:尼氟酸。(B)HaCaT细胞中的平行记录。
这一定位本身就具有重要意义。PACC1(也称PAC通道)是近年来才被克隆鉴定的新型氯离子通道,此前的研究主要集中在神经系统的痛觉感知领域,在皮肤生物学中的角色几乎是空白。
02
从感知到行动:PACC1如何触发脱屑级联反应
找到感受器只是第一步,更重要的是弄清楚它如何将酸性信号转化为生物学效应。
研究团队设计了一套严密的功能验证体系。在pH 5.6刺激2小时、继续培养24小时后,野生型细胞中KLK5和KLK7的蛋白水平显著上升,同时桥粒蛋白DSG1和DSC1的水平下降——这正是酸促进脱屑的经典分子特征。而在PACC1敲低细胞中,这些变化被大幅逆转。药理学抑制剂C77304(一种选择性PACC1拮抗剂)也产生了相同的效果,排除了非特异性影响的可能。
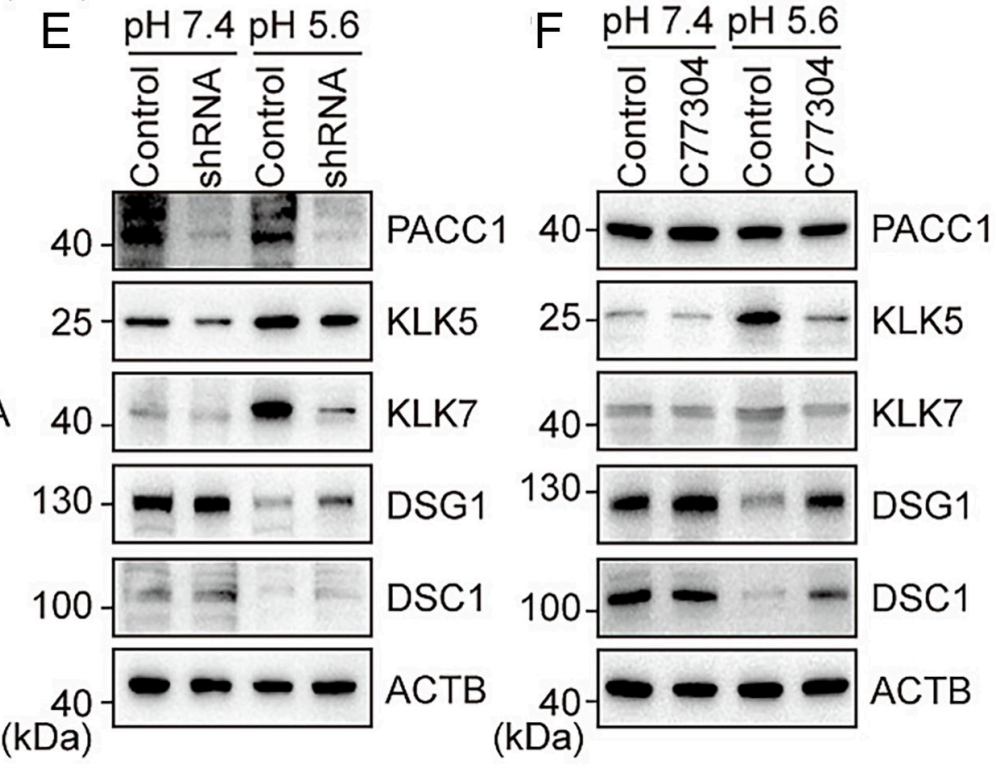
图1. (E)在不同pH条件下,野生型和PACC1敲低HaCaT细胞中PACC1、KLK5、KLK7、DSG1和DSC1的表达水平。
(F)在不同pH条件下,使用或不使用300 μM C77304时,HaCaT细胞中PACC1、KLK5、KLK7、DSG1和DSC1的表达。
更精妙的是质子感知突变体实验。研究者用CRISPR/Cas9构建了PACC1敲除细胞系,再分别导入野生型PACC1和三种质子感知位点突变体(E181A、E257A、E261A)进行功能回补。结果清楚表明:只有野生型PACC1能恢复酸诱导的KLK上调,三种突变体均无效。这说明PACC1发挥作用依赖于它感知胞外质子的能力,而非仅仅是通道蛋白的物理存在。ELISA实验进一步证实,PACC1敲除细胞在酸性刺激下分泌到胞外的KLK5/7也显著减少,意味着PACC1不仅调控KLK的表达,还影响其分泌。
03
信号通路:氯离子外流如何抵达基因转录
PACC1激活后,下游信号如何传递到细胞核并调控KLK基因转录?这是理解整个通路不可回避的问题。
研究团队对多条候选信号通路进行了系统筛查,包括PI3K-Akt、MEK/ERK、IL-17、STAT5和TGF-β/Smad通路,结果均为阴性。唯一有效的是AP-1抑制剂T-5224——它能显著阻断酸诱导的KLK5/7上调。沿着这条线索向上追溯,酸性刺激在野生型细胞中明显促进了JNK和c-Jun(AP-1的上游激酶)的磷酸化,而这一效应在PACC1敲除细胞中几乎消失。JNK和JUN的单独敲低同样足以阻断酸诱导的KLK上调。
至此,一条完整的信号轴得以建立:胞外酸性→PACC1感知质子→氯离子外流→JNK磷酸化→AP-1激活→KLK5/7转录上调→桥粒蛋白降解→角质细胞脱落。
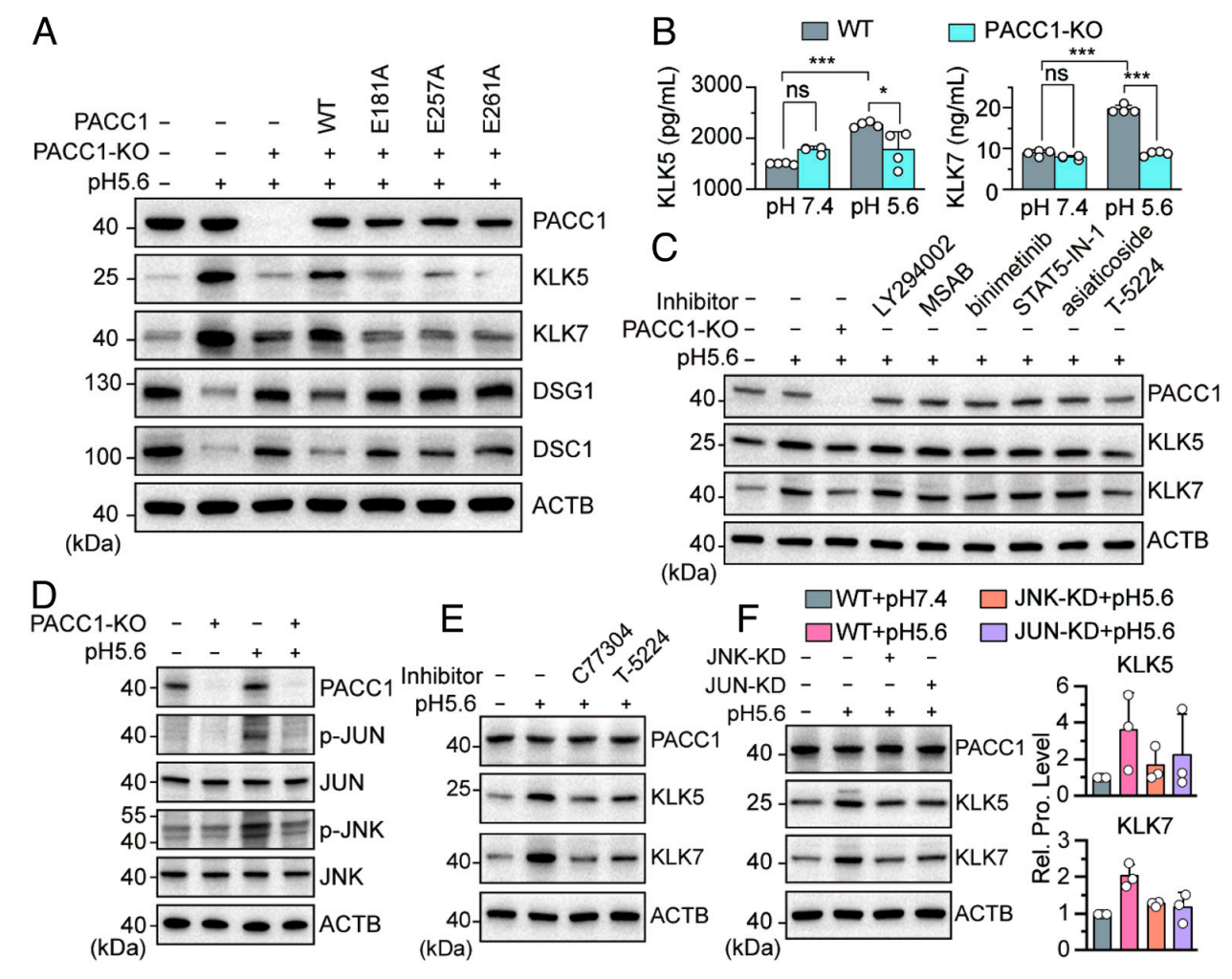
图2. (D)酸性刺激及PACC1对JUN和JNK磷酸化的影响。F)不同pH条件下,JUN和JNK敲低的人角质形成细胞中PACC1及KLK5/7的表达。
值得注意的是,氯离子外流如何激活JNK这一环节尚未完全阐明。研究者提出了几种可能机制:氯离子浓度变化直接解除对上游JNK激酶的抑制;细胞容积变化触发机械敏感信号;以及Ca²⁺、Mg²⁺等二价阳离子稳态的改变。这一”黑箱”的存在,既是研究的局限,也是后续探索的方向。
04
对现有脱屑模型的补充与意义
皮肤脱屑的经典模型聚焦于角质层内的LEKTI-KLK调控:在角质层深层,LEKTI与KLK结合并抑制其活性;随着pH向表面降低,LEKTI解离,KLK被激活,促进脱屑。这是一个发生在已分化、无核角质细胞层面的”被动”调控机制。
本研究提出的PACC1-JNK-AP-1通路则代表了一个”主动”的补充层次:活的角质形成细胞能够主动感知胞外pH下降,并通过转录调控提前上调KLK的表达和分泌,为后续的角质层脱落”预做准备”。两条通路协同运作,共同维持表皮稳态。
从应用层面看,这一发现的价值同样不容忽视。目前化学换肤(果酸、水杨酸等)的作用机制是非选择性地降低皮肤pH,在促进脱屑的同时往往伴随屏障损伤的风险。PACC1作为一个可药物靶向的离子通道,理论上可以实现更精准的脱屑调控——激动剂可强化脱屑,拮抗剂则可用于过度脱屑相关疾病(如特应性皮炎、银屑病)的治疗。当然,从细胞实验到临床应用还有相当长的路要走,研究者也坦诚指出现有2D培养体系不能完全模拟表皮的分层角化过程,三维有机皮肤模型和人体皮肤样本的验证是必要的后续步骤。
发稿/咨询/合作联系:13710470565(微信)
相关文章